Contoh ikatan kovalen polar. Ikatan kovalen yang terbentuk antara atom dari jenis yang sama biasanya non.
Ikatan Kimia Diusun Oleh Ppt Download
Senyawa ionik terbentuk oleh transfer elektron yang bermuatan.
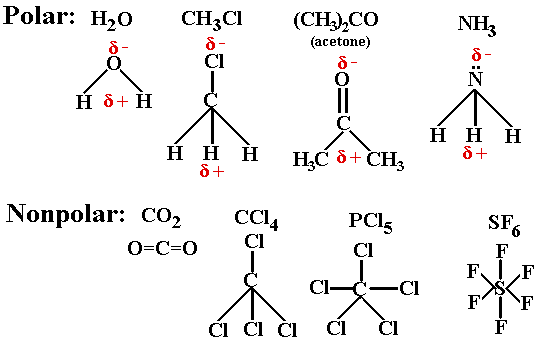
. Misalnya pada senyawa HF dimana elektron bersamanya digunakan secara tidak seimbang oleh kedua inti atom H dan inti atom F. Jumlah atom 2 harus berbeda. Ikatan kovalen polar Terbentuk antara atom yang memiliki perbedaan keelektronegatifan.
Pada molekul yang atom penyusunnya sejenis contohnya pada molekul H 2 hal ini disebabkan tidak ada perbedaan keelektronegatifan. Adik adik mesti tau bahwa Ikatan kovalen polar ini terjadi karena pasangan elektron ikatan tertarik lebih kuat ke salah satu atom. Contohnya meliputi Air HF dan CHF 3.
Sebuah senyawa terjadi ikatan kovalen polar apabila ada perbedaan kelektronegatifan yang mengakibatkan terjadinya pengutuban muatan. Hal ini terjadi karena antara dua atom F dan F memiliki keelektronegatifan yang sama besar atau perbedaan elektronegativitas adalah nol. Dapat terbentuk apabila unsur-unsur yang bereaksi mempunyai perbedaan daya tarik elektron yang cukup besar Perbedaan yang besar memungkinkan terjadi serah-terima.
Senyawa kovalen memiliki ikatan kovalen. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Tapi kemudian menjadi membosankan ketika Anda bertemu dan belajar sifat-sifat kimia ikatan kimia tabel unsur dan seterusnya dan sebagainya.
H2 N2 F2 2 Pasangan Elektron Bebas PEB Atom pusat memiliki pasangan elektron bebas PEB. Contohnya termasuk Pentana Heksana dan Karbon Dioksida. Pengertian dan Tata Nama Senyawa.
Berdasarkan kepolarannya senyawa kovalen terbagi menjadi senyawa kovalen polar dan senyawa kovalen non polar. Kepolaran pada molekul ini terjadi karena antara atom H dan atom Cl. Secara garis besar ikatan antar unsur dibedakan menjadi dua jenis yaitu ikatan logam dan ikatan kovalen.
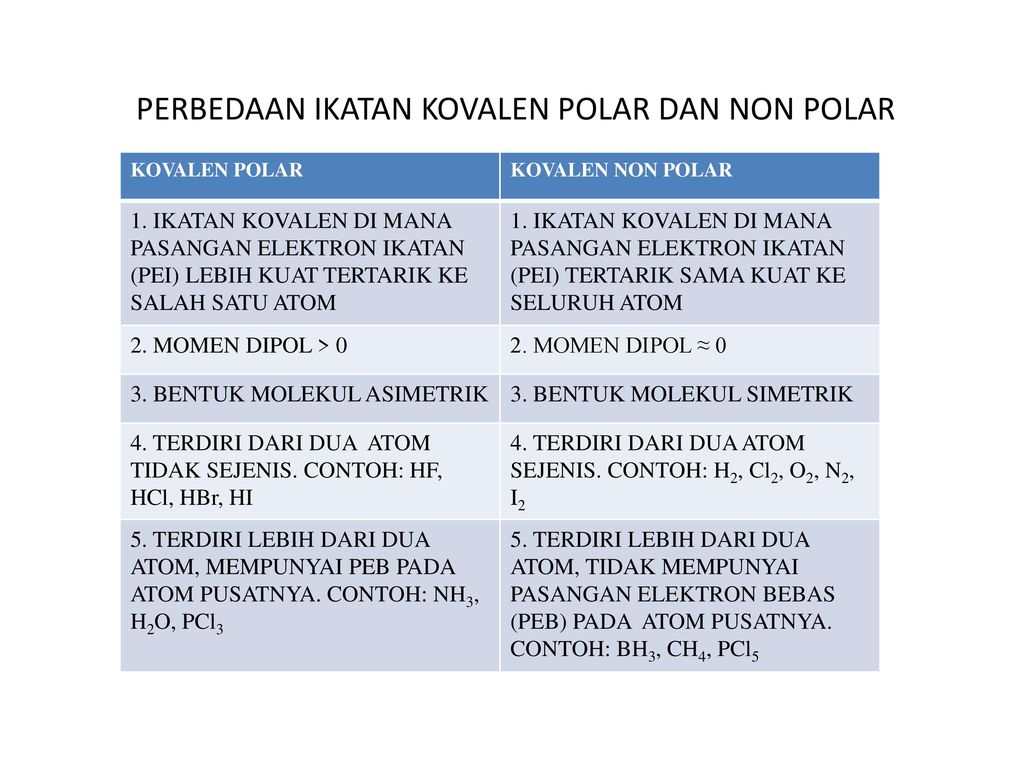
Jenis Ikatan Molekul. Perbedaan Ikatan Kovalen Polar Ikatan Kovalen Nonpolar 1 Keelektronegatifan Terdapat perbedaan keelektronegatifan. Kesetimbangan Ion dan pH Larutan Garam.
Senyawa kovalen polar dan nonpolar penyusunnya. HF HCl dan HBr. Ikatan kovalen non-polar Dibentuk oleh atom yang identik.
Pada contoh ikatan kovalen polar yaitu pada molekul HCl pasangan elektron ikatan PEI cenderung tertarik ke salah satu atom yang memiliki elektronegativitas lebih besar yaitu atom Cl oleh. Contoh senyawa kovalen nonpolar yaitu H 2 O 2 N 2 Cl 2 CH 4 C 6 H 6 dan BF 3. Senyawa kovalen polar dapat menghantarkan arus listrik dalam bentuk lelehannya.
Kovalen polar dan non polar dimasukkan dalam kelompok kovalen. Sebaliknya jika tidak memiliki perbedaan harga keelektronegatifam antar kedua atom yang berikatan maka akan semakin nonpolar ikatannya. Ikatan antara unsur-unsur ini beragam bergantung pada jenis unsur.
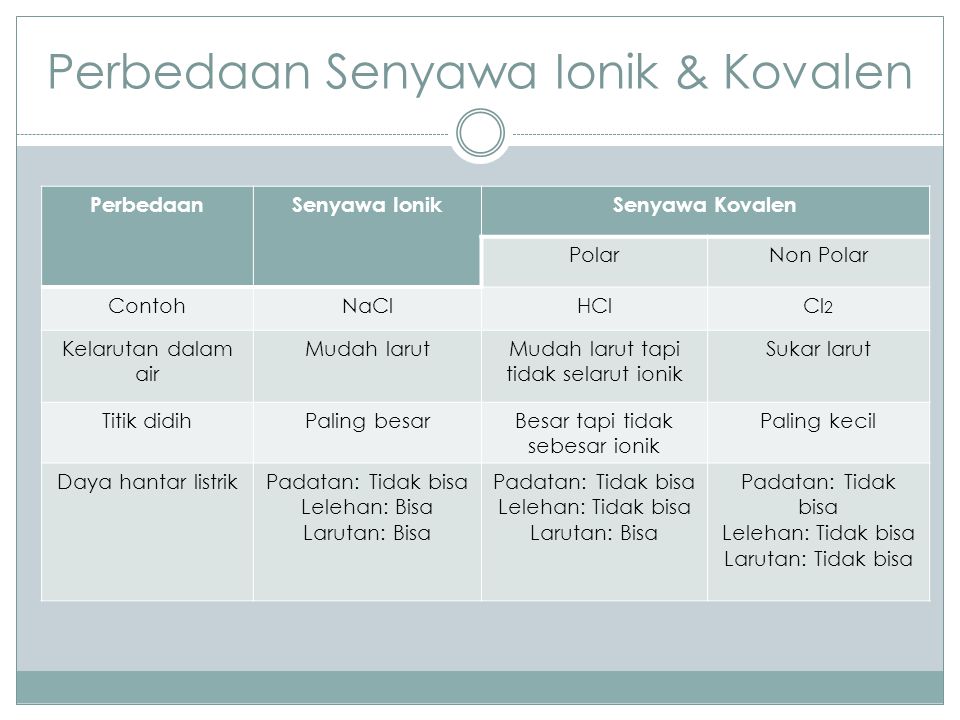
Ikatan ion membentuk senyawa ion sedangkan ikata kovalen membentuk senyawa kovalen. Senyawa ion dapat menghantarkan arus listrik dalam bentuk padatannya. Dalam ikatan kovalen dikenal dengan adanya ikatan kovalen nonpolar dan polar.
Struktur Tata Nama Sifat Penggunaan dan Penggolongan Makromolekul. Karena PEI tertarik sama kuat maka bentuk molekul pada senyawa F 2 adalah simetris. Ikatan kovalen nonpolar adalah ikatan kovalen yang pasangan elektron yang dipakai bersama tertarik sama kuat.
Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas. Perbedaan Ikatan Kovalen Polar dan Nonpolar. Hal ini karena air melarutkan zat polar yang merupakan konsistensi senyawa ionik sedangkan senyawa kovalen non-polar.
Makin besar selisih keelektronegatifannya makin besar pula kepolaran ikatan. Struktur Tata Nama Sifat Isomer Identifikasi dan Kegunaan Senyawa. Senyawa nonpolar memiliki titik didih rendah titik leleh tekanan uap tinggi dan tegangan permukaan rendah.
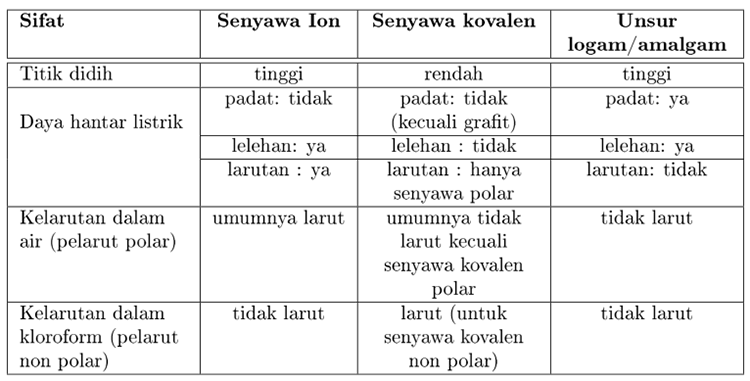
Penyataan yang tepat untuk membedakan senyawa ion kovalen polar dan kovalen nonpolar berdasarkan kemampuannya menghantarkan arus listrik adalah. Ada tiga jenis ikatan dalam molekulsenyawa yaitu ikatan ion ikatan kovalen polar dan kovalen non polar. 1Ikatan kovalen polar.
Ikatan yang terjadi antara ion-ion logam dan non logam Ikatan terbentuk akibat gaya tarik listrik antara ion yang berbeda Ikatan ion juga dikenal sebagai ikatan elektrovalen. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya. Contoh senyawa kovalen polar yaitu HCl HBr HI HF H 2 O dan NH 3.
Untuk membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar bisa ditunjukan dari beberapa sisi diantaranya dari ciri senyawa distribusi elektronnya dan ukuran kuantitatif titik didih. Pengertian Senyawa Nonpolar Pengertian Senyawa Polar. Senyawa tersebut terbentuk karena unsur-unsur saling berikatan.
Untuk lebih jelasnya silahkan anda simak uraian berikut ini semoga bisa memberikan pencerahan dalam. Senyawa kovalen koordinasi adalah ikatan kovalen di mana pasangan elektron yang dipakai bersama hanya disumbangkan oleh satu atom sedangkan atom yang satu lagi tidak menyumbangkan elektron. Adanya kepolaran ikatan disebabkan oleh perbedaan keelektronegatifan antarzat yang berikatan.
Perbedaan Senyawa Polar dengan Non Polar. Senyawa-senyawa kovalen dengan ikatan kimia dengan kovalen nonpolar maka tidak ada muatan parsial baik positif maupum negatif. Pada contoh ikatan kovalen polar yaitu pada molekul HCl pasangan elektron ikatan PEI cenderung tertarik ke salah satu atom yang memiliki elektronegativitas lebih besar yaitu atom Cl oleh karena itu bentuk molekulnya mengutub pada atom Cl sehingga menjadi asimetris tidak simetris.
Senyawa ion juga lebih larut dalam air dibandingkan senyawa kovalen. Ketika kita pertama kali tahu tentang kimia sebagian besar dari kita menemukan itu menyenangkan dan menarik. Perhatikanlah gambar berikut ini.
Atom N pada molekul amonia NH3 mempunyai. Senyawa kovalen tidak memiliki kemampuan ini karena mereka tidak mengandung ion. Untuk lebih memahami ikatan kovalen polar dan nonpolar pada suatu senyawa perhatikan ilustrasi berikut ini.
Tidak terdapat perbedaan keelektronegatifan. Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion-ionnya sehingga dapat menghantarkan arus listrik. Sekarang kami akan bahas sedikit tentang apa perbedaan antara Senyawa dengan ikatan kovalen polar dan non polar.
Sebutkan 8 Perbedaan Senyawa Polar dan Nonpolar. Kita merasa frustrasi harus menghafal sifat. Ikatan kovalen koordinasi hanya dapat terjadi jika salah satu atom mempunyai pasangan elektron bebas PEB.
SMALarutan Elektrolit dan. Misalnya Cl 2 O 2 N 2 dll. H 2 O HI HCl NH 3.
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

Ikatan Kovalen Polar Dan Nonpolar Penjelasan Perbedaan Dan Contoh

Jelaskan Perbedaan Antara Senyawa Polar Dengan Nonpolar Dan Berikan Masing Masing Contohnya Brainly Co Id

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id

Perbedaan Polar Dan Nonpolar Apayangdimaksud Com

Sebutkan 8 Perbedaan Senyawa Polar Dan Nonpolar Konsep Pentingnya Usaha Tiga Dua Satu

Sebutkan 5 Contoh Perbedaan Antara Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya
Perbedaan Ikatan Kovalen Polar Dan Non Polar Ppt Download

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom

1 Senyawa Kovalen Polar Dan Non Polar Ppt Download
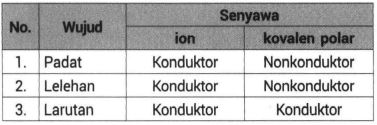
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

4 Perbedaan Ikatan Kovalen Polar Dan Non Polar Materi Kimia
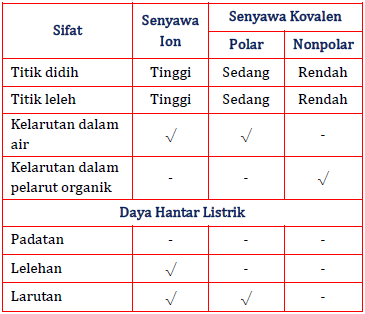
Jenis Ikatan Yang Terdapat Dalam Zat X Dan Y Bertu

